在當(dāng)今數(shù)字化時(shí)代,企業(yè)網(wǎng)頁設(shè)計(jì)不僅是品牌形象的展示窗口,更是吸引用戶、提升用戶體驗(yàn)的關(guān)鍵工具。休閑度假主題的簡約版式網(wǎng)頁設(shè)計(jì),以其清新自然的風(fēng)格和高效的實(shí)用性,成為眾多企業(yè)青睞的選擇。本文將探討休閑度假簡約版式WEB網(wǎng)頁設(shè)計(jì)的特點(diǎn)、優(yōu)勢,以及如何利用PSD素材和網(wǎng)頁模板來簡化設(shè)計(jì)流程,助力企業(yè)打造專業(yè)且吸引人的在線平臺(tái)。
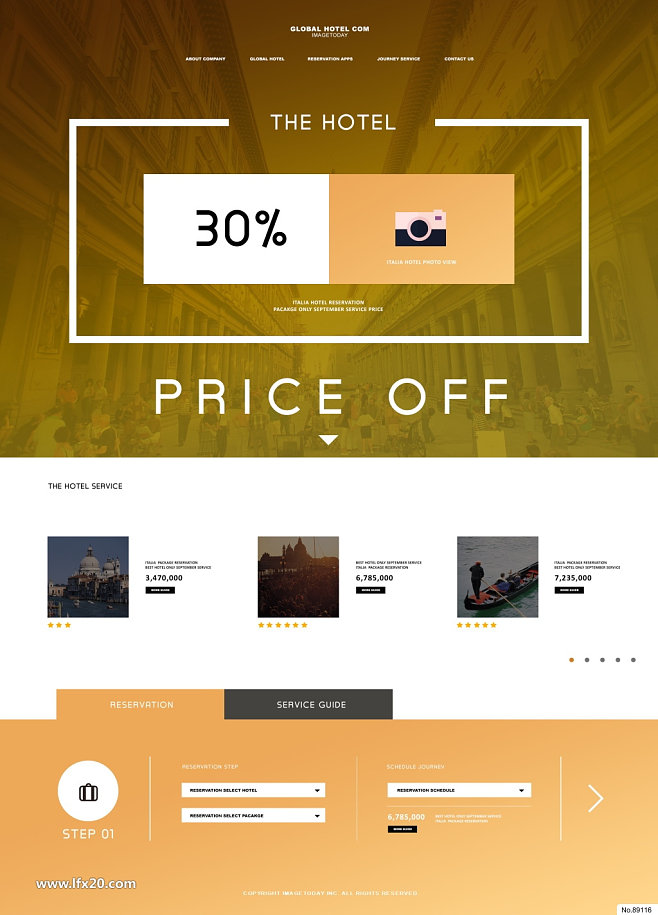
休閑度假簡約版式設(shè)計(jì)的核心理念在于融合輕松愉悅的度假氛圍與極簡主義的美學(xué)原則。這種設(shè)計(jì)風(fēng)格通常采用柔和的色調(diào),如淺藍(lán)、米白或自然綠,搭配簡潔的布局,避免過多裝飾元素,以突出內(nèi)容的清晰度。例如,在網(wǎng)頁模板中,大圖背景展示度假場景(如海灘、森林或酒店),配合簡約的導(dǎo)航欄和按鈕,讓用戶一目了然地獲取信息。這種設(shè)計(jì)不僅視覺上舒適,還能快速傳達(dá)企業(yè)(如旅游公司、度假村或相關(guān)服務(wù)提供商)的核心價(jià)值。
使用PSD素材和網(wǎng)頁模板可以大幅提升設(shè)計(jì)效率。PSD(Photoshop Document)素材提供了分層文件,允許設(shè)計(jì)師輕松自定義顏色、字體和布局,而無需從零開始。對(duì)于企業(yè)而言,選擇預(yù)先設(shè)計(jì)的休閑度假主題模板,可以節(jié)省時(shí)間和成本,同時(shí)確保設(shè)計(jì)的一致性。例如,一個(gè)典型的簡約版式模板可能包含響應(yīng)式布局,適應(yīng)不同設(shè)備屏幕,以及模塊化部分如介紹、服務(wù)列表和聯(lián)系表單。這些元素通過PSD文件進(jìn)行精細(xì)調(diào)整,幫助設(shè)計(jì)師快速實(shí)現(xiàn)品牌個(gè)性化,同時(shí)保持整體的簡約美感。
在優(yōu)勢方面,休閑度假簡約版式設(shè)計(jì)強(qiáng)調(diào)用戶體驗(yàn)。通過減少視覺干擾,它引導(dǎo)用戶專注于關(guān)鍵內(nèi)容,如產(chǎn)品詳情、預(yù)訂選項(xiàng)或企業(yè)故事,從而提升轉(zhuǎn)化率。研究表明,簡約設(shè)計(jì)能降低頁面加載時(shí)間,提高訪問速度——這對(duì)移動(dòng)用戶尤為重要。這種風(fēng)格易于維護(hù)和更新,企業(yè)可以基于模板定期刷新內(nèi)容,保持網(wǎng)頁的活力。
實(shí)施過程中也需注意平衡簡約與信息豐富性。過度簡化可能導(dǎo)致內(nèi)容缺失,因此設(shè)計(jì)師應(yīng)利用PSD素材的靈活性,添加必要的交互元素,如懸停效果或動(dòng)畫,以增強(qiáng)參與感。同時(shí),確保設(shè)計(jì)與品牌調(diào)性一致,例如,度假企業(yè)可融入自然圖標(biāo)或溫馨字體,強(qiáng)化休閑主題。
休閑度假簡約版式WEB網(wǎng)頁設(shè)計(jì)結(jié)合了美學(xué)與功能性,是企業(yè)提升在線存在的有效策略。通過借助PSD素材和網(wǎng)頁模板,設(shè)計(jì)師可以高效地創(chuàng)建出既專業(yè)又親切的網(wǎng)頁,吸引更多潛在客戶。無論是初創(chuàng)公司還是成熟企業(yè),這種設(shè)計(jì)方法都能在競爭激烈的數(shù)字市場中脫穎而出,為用戶帶來愉悅的瀏覽體驗(yàn),從而推動(dòng)業(yè)務(wù)增長。